2026年2月20日、日本の医療界のみならず世界中の科学コミュニティが震える歴史的な決定が下されました。厚生労働省の専門家部会は、iPS細胞(人工多能性幹細胞)を用いた再生医療製品2品目の製造販売を、世界で初めて了承したのです。
2006年に京都大学の山中伸弥教授がマウスでiPS細胞を樹立してからちょうど20年。2012年のノーベル生理学・医学賞受賞から14年。ついに「夢の医療」が研究室の顕微鏡を飛び出し、一般の患者が治療として受けられる「製品」へと進化を遂げました。今回の承認は、単なる新薬の登場ではありません。人類が「失われた臓器の機能を取り戻す」という、これまでの医療の常識を根底から覆す「ヤバイ医療革命」の幕開けなのです。
iPS細胞、ついに「製品」へ:山中伸弥教授の樹立から約20年、夢が現実に
これまでの再生医療の多くは、患者自身の細胞を採取して加工する「自家細胞」によるものでした。しかし、今回の承認が革命的なのは、あらかじめ作っておいたiPS細胞から大量に細胞を分化させ、それをパッケージ化した「他家細胞(ストック型)」の製品であるという点です。これにより、治療が必要な時にすぐに提供できる「工業製品」としての再生医療が現実のものとなりました。
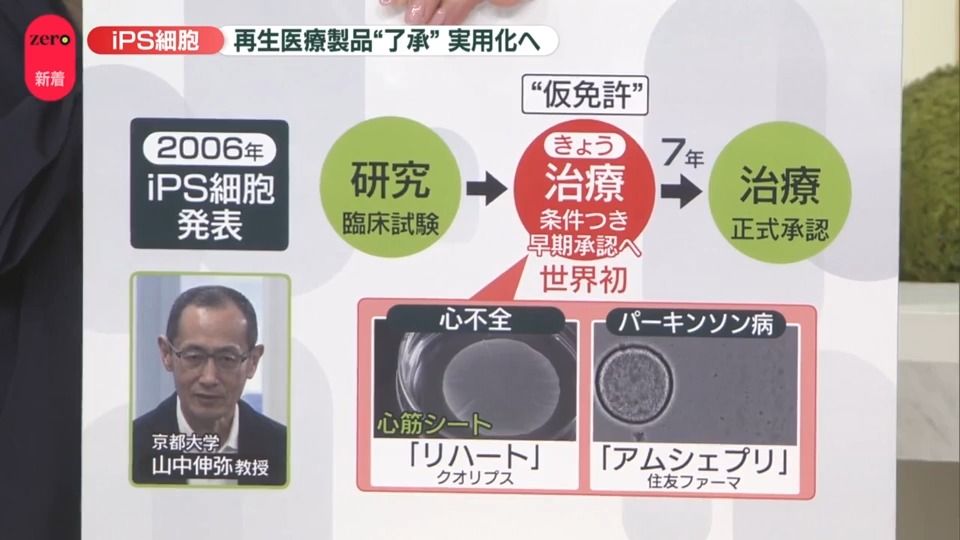
「アムシェプリ」と「リハート」:世界が注目する2大再生医療製品の全貌
今回承認されたのは、以下の2つの革新的製品です。
| 製品名 | 開発企業 | 対象疾患 | 治療の内容 |
|---|---|---|---|
| アムシェプリ | 住友ファーマ | パーキンソン病 | iPS細胞由来のドパミン神経前駆細胞を脳内に移植 |
| リハート | クオリプス | 重症心不全 | iPS細胞から作った純度の高い心筋細胞をシート状にして貼付 |
「ヤバイ医療革命」と言われる理由:これまでの対症療法とは次元が違う
従来の医療は、悪くなった部分の症状を和らげる「対症療法」が主流でした。例えば心不全なら心臓の負担を減らす薬を飲み、パーキンソン病なら不足した物質を薬で補う。しかし、これらは「壊れた細胞」を直すものではありません。iPS細胞による治療は、死滅した細胞そのものを「新しい生きた細胞」で置き換えます。つまり、壊れたエンジンを修理するのではなく、新品のエンジンパーツに交換するような次元の違うアプローチなのです。
70年ぶりの大進化!失われた機能を取り戻す「再生」の時代が到来
医学の歴史において、抗生物質の発見やワクチンの普及、臓器移植の確立など、数十年単位でパラダイムシフトが起こります。今回のiPS細胞製品の承認は、1954年の世界初の腎移植成功以来、約70年ぶりの「臓器修復における大進化」と言っても過言ではありません。
パーキンソン病治療の常識が崩壊。iPS由来製品「アムシェプリ」がもたらす希望
パーキンソン病は、脳内の「ドパミン」を作る神経細胞が徐々に減っていくことで、体が思うように動かなくなる難病です。日本国内だけでも約20万人の患者がいると推定されています。
「震え」や「すくみ」の原因、ドパミン神経を直接補充する凄さ
これまでの標準治療は「L-ドパ」などの薬剤を服用し、脳内のドパミン濃度を維持することでした。しかし、病気が進行すると薬の効果が持続しなくなる「ウェアリング・オフ現象」に悩まされます。アムシェプリは、iPS細胞から作製した「ドパミン神経前駆細胞」約500万個を、脳の「線条体」という部分に直接移植します。移植された細胞が脳内で成熟し、自らドパミンを放出し続けるため、薬に頼り切らない状態を目指せます。
住友ファーマ×京都大学のタッグが生んだ世界初の実績
この製品は、京都大学iPS細胞研究所(CiRA)の髙橋淳教授らの研究成果をベースに、住友ファーマが商用化したものです。他人のiPS細胞を使用するため、拒絶反応を抑えるために免疫型(HLA)を合わせた細胞ストックが活用されています。
医師主導治験で見えた確かな手応え:安全性と有効性の示唆
京都大学附属病院で行われた治験では、以下の結果が報告されています。
- 安全性: 移植手術に伴う重大な合併症や、細胞の腫瘍化(ガン化)は認められませんでした。
- 有効性: 運動機能の評価指標において、移植後に症状の改善や進行の抑制が示唆されました。特に、薬の効果が切れる時間が短縮されるなど、生活の質(QOL)の向上が確認されています。
一生薬を飲み続ける生活から根本的な改善へのシフト
アムシェプリが普及すれば、患者は毎日数時間おきに薬を飲むストレスから解放される可能性があります。完全に薬がゼロになるわけではありませんが、「動けない時間(オフタイム)」が劇的に減ることは、患者にとって人生を取り戻すに等しい変化です。
重症心不全の「ラストリゾート」。クオリプス社の心筋シート「リハート」
心不全は、心臓のポンプ機能が低下し、全身に十分な血液を送れなくなる状態です。重症化すると、残された道は補助人工心臓の装着か、ドナーを待つ心臓移植しかありませんでした。
心臓移植を待つしかない患者への光:iPS由来の「動くシート」
クオリプス社が開発した「リハート」は、iPS細胞から分化させた心筋細胞を約数千万個使い、直径数センチの薄い「シート」状に加工したものです。これを弱った心臓の表面に直接貼り付けます。
慶應義塾大学名誉教授らによる世界初の治験成果
慶應義塾大学の福田恵一名誉教授らのチームが実施した治験では、拡張型心筋症などの重症患者に対し、劇的な改善効果が見られました。
- ポンプ機能の回復: 血液を送り出す能力(左室駆出率)が、移植前と比較して有意に上昇。
- 心機能の維持: シートから分泌されるサイトカイン(成長因子)が、元々あった心筋の再生を促し、血管を新生させる「パラクライン効果」も確認されました。
なぜシート状なのか?「物理的な再生」の仕組み
心筋細胞をバラバラの状態で注入するのではなく、シート状にすることで、細胞が心臓に定着しやすくなります。このシートは心臓の拍動と同期して動くため、物理的な補助としても機能します。
心不全による「入退院の繰り返し」を終わらせる可能性
重症心不全患者の多くは、少しの負荷で息切れし、頻繁に入退院を繰り返します。リハートの投与により、日常生活を自立して送れるレベルまで回復すれば、医療経済的にも、患者の精神的負担においても、その価値は計り知れません。
「条件・期限付き承認」という日本の超速戦略。なぜ世界最速なのか?
今回の承認は、正式には「条件・期限付き承認」です。これは日本が世界に先駆けて導入した、再生医療のための特殊な制度です。
2026年2月、厚労省・薬事審議会での歴史的決断
通常、医薬品の承認には大規模な「第3相試験(フェーズ3)」が必要で、数千人規模のデータと10年以上の膨大な時間がかかります。しかし、再生医療は対象患者が少なかったり、既存の枠組みでは評価が難しかったりします。そこで「安全性」が確認され、「有効性」が推定できれば、先行して販売を認めるという決断がなされました。
最大7年間の期限付きで製品を市場に出すメリット
この制度により、最大7年間の期限付きで製品を市場に出すことができます。
- メリット: 患者は数年早く最新治療を受けられる。
- 課題: 7年以内に改めて有効性を証明できなければ、承認は取り消される。
欧米を出し抜いた日本の「薬機法」の仕組み
アメリカ(FDA)や欧州(EMA)にも早期アクセス制度はありますが、日本の「医薬品医療機器等法(薬機法)」に基づくこの制度は非常に柔軟です。これにより、世界中の再生医療ベンチャーが日本を「最初の市場」として選ぶようになっています。
| 制度比較 | 日本(再生医療等製品) | 海外(一般的な特例) |
|---|---|---|
| 承認のタイミング | フェーズ2終了後(有効性推定段階) | 原則フェーズ3終了後 |
| 期限の設定 | あり(最長7年) | なし(または追加要件のみ) |
| 狙い | 世界最速の実用化と市場形成 | 安全性の完全確保 |
現場の口コミ・評判は?iPS再生医療製品に期待する声と不安な本音
患者・家族の切実な声:「やっとここまで来た」
SNSや患者会では、「山中先生がiPS細胞を見つけた時からずっと待っていた」「治らないと言われた病気に光が見えた」という感動の声が溢れています。特に20代、30代で発症した若年性パーキンソン病の患者にとって、このニュースは「人生の再設計」を可能にする福音です。
医療従事者の視点:期待と慎重論
医師からは「画期的な手段が増えた」と歓迎される一方、「どのタイミングでこの治療を提案すべきか」というガイドラインの整備を求める声もあります。手術が必要な治療法であるため、実施できる病院の選定も今後の課題となります。
投資家・ビジネス界の反応:数千億円規模の市場創出
クオリプスや住友ファーマの株価は、承認報道を受けて敏感に反応しました。野村総合研究所などの予測では、2030年までに国内の再生医療市場は数千億円規模に達するとされており、日本が科学技術で外貨を稼ぐ新たな産業の柱として期待されています。
iPS細胞で「次に治る病気」は何か?脊髄損傷、糖尿病、眼疾患への展望
今回承認された2品目は「先陣」に過ぎません。iPS細胞の真価は、全身のあらゆる細胞になれる多能性にあります。
脊髄損傷:車椅子生活からの脱却を目指す最新研究
慶應義塾大学の岡野栄之教授らのチームが、iPS細胞から作った神経前駆細胞を脊髄損傷患者に移植する治験を進めています。感覚の回復や、わずかな足の動きが確認されるなど、リハビリテーションとの組み合わせによる劇的な改善が期待されています。
糖尿病:インスリン注射が不要になる未来
1型糖尿病など、インスリンを作る細胞が壊れてしまう疾患に対し、iPS細胞から作った「膵島細胞」を移植する研究が進んでいます。これが実現すれば、毎日の血糖値測定とインスリン注射という重荷から患者を解放できます。
眼疾患(網膜再生):量産化・製品化への壁
理化学研究所の高橋政代氏らが世界で初めてiPS細胞を人に応用したのは、目の難病「加齢黄斑変性」でした。この分野は先行しているため、より安価で使いやすい既製品(他家細胞)としての承認が待たれます。
高額治療の壁をどう乗り越える?数千万円のコストと保険適用の課題
再生医療はなぜ高い?複雑な製造工程の裏側
再生医療製品は、一般的な錠剤のように化学合成で作れるものではありません。生きている細胞を、高度なクリーンルーム(CPC)で、熟練の技術者が数ヶ月かけて培養します。
- コストの理由1: 厳格な無菌検査と遺伝子異常チェックのコスト。
- コストの理由2: 輸送時の徹底した温度管理とスピード。
今後の量産化で価格は下がるのか?
現在の予想価格は、1回の治療で1,000万円〜3,000万円以上になると見られています。しかし、自動培養装置の導入や、共通のiPS細胞ストックの活用が進めば、10年後には現在の半額以下になる可能性があります。
「未来への投資」としての再生医療
一見、高額に見える治療費ですが、もし寝たきりの患者が自立し、仕事に復帰できれば、長期的な介護費用や社会保障費の削減につながります。これは単なる「医療費の支出」ではなく、社会全体としての「未来への投資」なのです。
まとめ:iPS細胞の実用化は、人類が「老化」と「損傷」を克服する第一歩
2026年2月、私たちは医療の歴史が塗り替えられる瞬間を目の当たりにしました。iPS細胞を用いた「アムシェプリ」と「リハート」の承認は、もはやiPS細胞が「未来の技術」ではなく、今この時を生きる私たちのための「現実の選択肢」になったことを意味します。
もちろん、コストや長期的な安全性など、解決すべき課題はまだ山積みです。しかし、20年前に山中教授が蒔いた一粒の種は、多くの研究者、企業、そして勇気を持って治験に参加した患者たちの手によって、大きな大樹へと成長しました。
これからの私たちにできること
- 正しい知識を持つ: 誇大広告や未承認の怪しい自由診療に惑わされないよう、公的な情報を確認しましょう。
- 制度を支援する: 再生医療への公的投資や、寄付、治験への理解を深めることが、次の難病治療を早めます。
日本の科学技術が世界をリードするこの「医療革命」。次は、あなたの、あるいは大切な誰かの命を救う番かもしれません。

コメント